INTRODUCCIÓN
Es la industria farmacológica una de las más
poderosas e influyentes en la vida humana,
y el avance tecnológico la ha llevado de la
mano porque siempre ha estado en constante
desarrollo. Esta imparable área de la
investigación científica, tiene sus cimientos
en innumerables recursos humanos, profesionales
que se han comprometido con la
investigación, básicamente, experimental.
La formación de profesionales en el área de
farmacología, incluyendo médicos, enfermeras
y demás profesionales de la salud,
debería ser un asunto serio y en el que no
debería escatimarse en gastos tanto materiales
como intelectuales. Sin embargo, no
todas las instituciones cuentan con el máximo
aporte o recurso disponible para llevar a
cabo su labor de manera óptima.
Las instituciones públicas que se dedican
al estudio farmacológico están siempre
orientadas a la salud pública y a la alimentación,
cuentan con apoyo financiero suficiente
según la capacidad de cada país. Los
países desarrollados tienen mucho avance
farmacológico mientras que los países más
pobres o en vía de desarrollo cuentan con
nada o casi nada para financiar sus estudios
experimentales.
Por otro lado, las instituciones privadas son
movidas por intereses lucrativos y su capital
les permite la avanzada en estudios
farmacológicos. Ni hablar de las grandes
trasnacionales farmacéuticas que imperan
en recursos de todo tipo para el desarrollo
constante del área.
Todas las universidades del mundo que
tienen una facultad de medicina o de farmacología,
tienen seguro un departamento
dedicado a la investigación y práctica
farmacológica. No todas las universidades
cuentan con el máximo de recurso posible
y de vanguardia para desarrollar los estudios
de farmacia, pero por lo menos deben
contar con el incentivo investigativo para
promocionar el experimento del área en
cuestión.
En base a esto, los profesores, estudiantes
y personal de laboratorio de la Facultad
de Ciencias Médicas de la Universidad de
Guayaquil, proponen un Manual de Prácticas
Experimentales que incentiven la investigación
farmacológica y promueva la
mejora de las marchas y procedimientos
experimentales de la cátedra.
En tal sentido, el objetivo que se persigue
consiste en reprogramar el Manual de Prácticas
Experimentales de Farmacología y
promover una nueva cultura en el trabajo
de investigación farmacológica. Serán necesarios
experimentos más útiles que contemplen
las drogas actuales, y para ello, se
deberá disponer de los instrumentos y equipos
indispensables para llevar a cabo los
experimentos, así como la disposición de
reactivos y materiales incluyendo al material
biológico (animal).
El Manual de Prácticas Experimentales de
Farmacología permitirá que el estudiantado
sepa diferenciar el efecto terapéutico de
los fármacos y medicamentos y evalúe el
efecto biológico producido sobre aparatos
y sistemas, mediante el método científico y
siguiendo los procedimientos adecuados
de laboratorio. Es decir, el futuro profesional
de la Facultad de Ciencias Médicas de
la Universidad de Guayaquil, deberá estar
preparado para manejar los principales parámetros
de la farmacología:
a) Farmacocinética: Es “el paso de las drogas
a través del organismo en función del
tiempo y de la dosis. Comprende los procesos
de absorción, distribución, metabolismo
o biotransformación y excreción de las
drogas.” (Malgor & Valsecia, 2000, pág. 13)
b) Farmacodinámica: “es el estudio de los
efectos bioquímicos y fisiológicos de los
fármacos y sus mecanismos de acción. Los
efectos de casi todos los medicamentos son
consecuencia de su interacción con componentes
macromoleculares del organismo
son las acciones farmacológicas y los efec-
MANUAL DE PRÁCTICAS DE FARMACOLOGÍA
252 RECIMUNDO VOL. 4 Nº 1 (2020)
tos que producen los medicamentos en los
organismos humanos sanos y enfermos.”
(Hilal-Dandan, Randa ; Brunton, Laurence,
2013, pág. 29).
c) Mecanismo de Acción: “Es el conjunto de
procesos que se producen en las células,
debido a las acciones de las drogas sobre
el organismo. Las drogas tienen dos efectos
fundamentales sobre el organismo, estimular
o inhibir un proceso fisiológico. Los
fármacos no producen nuevas funciones
que el organismo no posee.” (Chéry, 2010).
d) Efectos colaterales y secundarios que
son los efectos distintos en el organismo a
dosis normales.
e) Intoxicación o efectos indebidos de los
fármacos en el organismo humano por dosis
elevadas o tóxicas (sobredosificación).
f) Contraindicaciones: son situaciones normales
o patológicas en las que no se puede
administrar un medicamento.
g) Interacciones medicamentosas: al interactuar
dos medicamentos pueden producir
sinergismo (aumento de la acción farmacológica
por la unión de dos drogas o
antagonismo (disminución de la acción farmacológica
por la adición de otra droga).
h) Preparados: Es la elección de la presentación
comercial de medicamentos más
adecuada.
i) Vías de administración: es la forma más
óptima para administrar la droga al paciente,
según el caso.
j) Dosificación: es la cantidad exacta necesaria
de un fármaco que se debe administrar
a un organismo sano o enfermo.
k) Indicaciones terapéuticas: Es la forma
como debe aplicarse un determinado fármaco
ante una enfermedad, además contempla
la población a quién es dirigida.
(niño, adulto, anciano).
Metodología
La propuesta presentó un enfoque cualitativo-
cuantitativo (mixto). Desde el punto
de vista cualitativo la desmotivación fue un
factor preponderante. Se evaluó la calidad
académica de la cátedra de farmacología
de la Facultad de Ciencias Médicas de la
Universidad de Guayaquil, comparando
con el nivel de preparación y experimentación
de otras instituciones en el mundo. De
esta manera se considera obsoleta la actual
estructura física, e insuficiente la cantidad
instrumental, material, de reactivos y bioteros.
Se realizaron encuestas y cuestionarios de
opinión sobre “las fallas pedagógicas en la
docencia experimental de farmacología”,
dónde la población a estudiar fueron los
docentes, estudiantes y personal de laboratorio
de la Facultad de Ciencias Médicas
de la Universidad de Guayaquil. Acompañando
la modalidad cuantitativa se aplicó
el método inductivo para analizar las características
de la población para llegar a conclusiones
generales.
Se realizó una exhaustiva revisión documental
para el diseño del Manual de Prácticas
Experimentales de Farmacología, la cual se
tomó como base para fundamentar las Marchas
Experimentales de Farmacología.
Luego de la realización de encuesta y su
cuestionario respectivo sobre las fallas pedagógicas
en la docencia experimental de
farmacología, aplicado sobre profesores,
estudiantes y personal de laboratorio totalmente
involucrados en el proceso enseñanza
aprendizaje, se obtuvieron los siguientes
resultados valorativos y cuantitativos:
- La mayoría considera inadecuadas las
clases magistrales: poco tiempo de 4
horas semanales.
- Se debe hacer un reajuste en el pensum
para la cátedra de farmacología.
- Se habla de una pobre comunicación
entre Estudiante y Profesor. Lo cual es
preocupante dada la importancia de ello
en el proceso de enseñanza y aprendizaje.
- Se necesita un reajuste en la evaluación
teórico-práctica.
- Se considera obsoleta la estructura física
del laboratorio.
- Escaso recursos materiales e Instrumentación.
- Insuficiente material biológico (ratones).
Es necesario la construcción de un biotero
con buena estructura y productividad.
- La mayoría coinciden en que las prácticas
experimentales y fármacos usados
deben actualizarse con tópicos útiles en
la vida diaria del médico de la comunidad,
quien tiene que resolver los problemas
de la salud y provisión de medicamentos.
A partir de estos resultados es que surge la
necesidad de diseñar un Manual de Prácticas
de Farmacología Experimental, para
llenar las aspiraciones de estudiantes, docentes
y personal de apoyo de laboratorio,
y como propuesta pedagógica, útil, actualizada
con medicamentos cuyos efectos colaterales
o secundarios sean minimizados
en lo posible:
Tabla 1. Manual de prácticas experimentales de farmacología de la Facultad de Ciencias
Médicas de la Universidad de Guayaquil
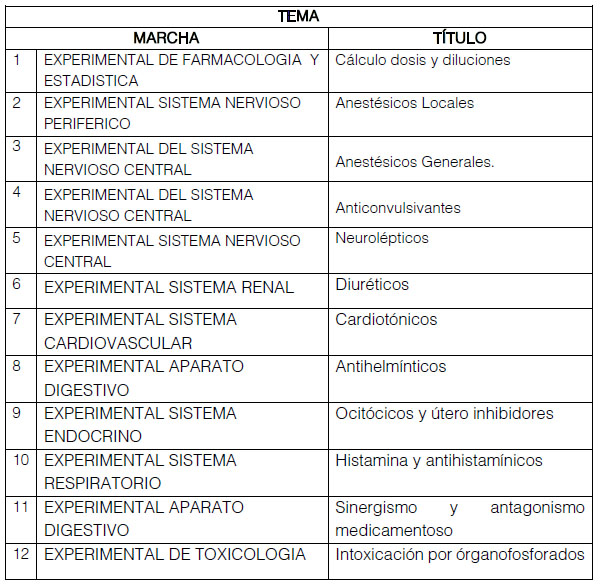
Fuente: Autores 2020
Marcha experimental de farmacologia y
estadistica
Cálculo de Dosis y Diluciones
Referencia Teórica:
“La farmacología puede definirse en un sentido
más amplio como el estudio de los medicamentos
que incluye su historia, origen,
propiedades físicas y químicas, presentación,
efectos bioquímicos y fisiológicos,
mecanismos de acción, absorción, distribución,
biotransformación, eliminación y usos
con fines terapéuticos." (Chéry, 2010, pág.
3)
Por eso, el conocimiento físico químico básico
(peso, volumen) es condición básica
necesaria para la determinación de dosis
farmacológicas.
Medidas de Peso:
En Farmacología, se tomará como unidad
al gramo (g), que es la milésima parte del
Kilogramo. Las medidas de peso se pueden
escribir en forma decimal, exponencial,
números enteros o fraccionados, por esta
razón diremos que en general adquieren diferentes
expresiones matemáticas y todas
son equivalentes.
0,1 g = 100 mg = 10 cg = 0,10 g = 0,001 Kg = 1 x 10 – 4 Kg.
Si nos dicen que escribamos ¼ de miligramo sería: 0,00025 g o 0,25 mg
Calculo de Dosis Total: Al determinar la dosis
total necesaria en un paciente, es preciso
conocer previamente la dosis/Kg de
peso corporal, a la que llamaremos dosis
standard y seguidamente aplicamos una
regla de tres simple. Por ejemplo: Se desea
conocer la dosis total de ampicilina que
debe administrarse a un adulto que pesa 87
kg. Si la dosis standard es de 100 mg/Kg.
Cuánto deberá administrarse?

Simpliicando magnitudes, tenemos que X = 8700 ng= 8,7 g
Cuando se trata de posología infantil y no se despone de báscula, o se desconoce el peso del niño, podemos deducir artificialmente en una relación aproximada de dosis pediátrica, "DOSIS RELATIVA". Hay que señalar la sensibilidad o tolerncia de los niños a medicamentos utilizados en adultos.
Medidas de Volumen:
Farmacología se ha adoptado como unidad el Mililitro (ml), que es la milésima parte del litro que también puede ser representado como centímetro cúbico (cc). 1 ml = 1 cc
Soluciones y Titulación de Diluciones
Como concepto general, una solución es la combinación de un disolvente con un solu- to. En la mayoría de los casos, el disolvente líquido es agua destilada y el soluto o sus- tancia disuelta, es una sal o también, otro líquido.
Las soluciones pueden ser: Isotónicas, Hi- pertónicas o Hipotónicas, de acuerdo a la concentración del soluto en el solvente.
El título de una solución representa la canti- dad de una sustancia contenida en un volu- men de 1 cc (ml), 10 cc (1dl), o 1000 cc (1 litro). Ejemplo:
Una solución titulada al 5%, significa 5 gra- mos disueltos en 100 ml de solución (SOLU- CION PORCENTUAL)
Desarrollando tenemos que 0,5 g = 500 mg contenidos en 100 cc
Problemas:
1. Se desea conocer el equivalente mg/ml de una solución titulada al 3% en un volumen de 1 ml.
mg/ml = 3 x 10 x 1 ml = 30 mg/ml
2. Si la solución de dextrosa en agua viene al 0,45 %; cuántos mcg existen en 0,5 ml. ?
0,45 g
x |
100 ml
0,5 ml |
x = 0,00225 g
R= 2250 mcg hay en 0,5 ml. |
Dilusiones
En muchos probelmas farmacológicos, debido a que algunas soluciones son muy concentradas, o porque el volumen a administrarse es muy pequeño, es preciso añadir un determinado volumen de solvernte (volumen adicional) a un milímetro de solución necesaria, a base de la cual se extrae la dosis calculada en mg/ml. Ejemplo: Se dispone una solución al 10% ¿Cómo se procede para convertirla en una solución al 1%?
En el problema llamaremos:
- So = Solución original.
- otas/minutos. En otros casos se emp
- V1= Volumen de 1 ml de solución original
- V2= Volumen en ml que es necesario añadir a V1.
- Para obtener el volumen total:
- So= 10%
- Sn= 1%
Dosificación por Gotas:
Las soluciones en General se dosifican por venoclisis a diversa velocidad de gotas/minutos. En otros casos se emplean equipos
cuentagotas, cuando es de menor volumen.
En venoclisis:
1 ml será igual a 20 gotas.
1 gota = 3 microgotas (equipo volutrol)
1 ml/hora = (bomba de infusión)
Objetivo: Reconocer medidas de peso, volumen,
soluciones, diluciones, medidas caseras
y reducciones entre unidades.
Estrategia: Test diagnóstico. Conferencia-
Discusión. Evaluación y Protocolo
Experimental
Resultados: Detectar y realizar reducciones entre medidas de peso, volumen, dilucio- nes, soluciones, medidas caseras, etc.
Conclusiones: Reconocer medidas, dilucio- nes, soluciones y realizar correctamente las reducciones.
Marcha experimental sistema nervioso periferico
Anestésicos Locales.
Referencia Teórica:
“Los anestésicos locales se unen de manera
reversible a un receptor específico dentro
del poro de los conductos de Na+ en los
nervios y bloquean los movimientos iónicos
a través de esa abertura. Cuando se aplican
al tejido nervioso en concentraciones
apropiadas, los anestésicos locales actúan
en cualquier parte de tal sistema o en cualquier
tipo de fibra nerviosa, y bloquean de
modo reversible los potenciales de acción
en que se basa la conducción nerviosa. “
(Hilal-Dandan, Randa ; Brunton, Laurence,
2013).
Su mecanismo de acción “es el bloqueo
de los canales de sodio dependientes de
voltaje. El ion sodio tiene una función fundamental
en la generación del potencial de
acción.” (Chéry, 2010)
Objetivo: Demostrar como el anestésico
local inhiben la propagación del impulso
nervioso sobre la musculatura esquelética
(nervio peróneo lateral) al bloquear los neurorreceptores.
Estrategia: Test diagnóstico. Conferencia-
Discusión. Evaluación y Protocolo Experimental.
Reactivo Biológico: Rata albina.
Reactivos Farmacológicos: Lidocaina 1%
con epinefrina. Xilocaina 1% Fco 50ml ,
Éter , Uretano
Materiales e instrumental:
Electrodos bipolares de platino
Carrete de Ruthenford (estimulador eléctrico)
Instrumental de disección quirúrgica
Tabla de fijación del animal
Algodón - Jeringuillas
Balanza
Seda quirúrgica
Estilete
Procedimiento: Se anestesia al animal, luego Aplicar éter por vía inhalatoria Uretan 10% 1 sol 1mg por vía IP.
Se diseca el nervio peróneo lateral y la masa
muscular adyacente con seda trenzada localizar
un segmento del nervio.
a) Testigo, estimulación directa del nervio
hasta detectar el umbral de excitabilidad y
su respuesta.
b) Problema, se agregan varias gotas de lidocaina
en algodón, se espera 5 min. y se
estimula eléctricamente el nervio con el voltaje que anteriormente producía respuesta.
Resultados:
a) Testigo, umbral de excitabilidad por la
corriente eléctrica.
b) Respuesta flexión busca de la extremidad
posterior de la rata.
b) Respuesta flexión busca de la extremidad
posterior de la rata.
c) Problema aplicando el voltaje anterior de
excitabilidad.
Respuesta no hay umbral de excitabilidad
ni flexión brusca.
Nota: - Puede ser el lado derecho testigo
y el lado izquierdo problema .
Con un solo nervio peróneo lateral 1° testigo
Luego 2° problema.
Conclusiones: El anestésico local (lidocaína
1%) bloquea la conducción nerviosa
produciendo insensibilidad y no respuesta
motora.
Marcha experimental del sistema nervioso central
Anestésicos Generales.
Referencia Teórica:
“Los anestésicos generales producen dos
efectos fisiológicos importantes a nivel celular:
Los anestésicos por inhalación hiperpolarizan
las neuronas, efecto importante en
aquellas que actúan como“marcapasos” y
en circuitos que generan pautas o características.
Los anestésicos por inhalación y los que se
aplican por vía IV ejercen efectos sustanciales
en la transmisión sináptica y otros de
menor cuantía en la generación o propagación
de potenciales de acción.” (Hilal-Dandan,
Randa ; Brunton, Laurence, 2013, pág.
327)
Farmacocinética: Se absorben por todas
las vías pero como se realiza por vía intravenosa
se descarta la absorción. Los órga-
LITUMA PEÑARRETA, O., AVALOS MORENO, E., ZEA MORALES, A., & CASTRO GARCÍA, R.
RECIMUNDO VOL. 4 Nº 1 (2020) 257
nos que reciben la mayor cantidad de anestésico
son aquellos que son más irrigados
como cerebro, corazón, hígado y riñón lo
que explica la rapidez de la anestesia. Desde
la sangre pasa a las vísceras y tejidos
en gran cantidad cayendo la concentración
sanguínea. Se metaboliza el anestésico y
luego es excretado por la orina.
- Objetivos: Observar los distintos períodos de la anestesia etérea.
- Estrategia: Test diagnóstico. Conferencia-Discusión. Evaluación y Protocolo Experimental.
- Reactivo Biológico: Rata albina.
- Reactivo Farmacológico: Éter.
Materiales e Instrumental:
- Campana de vidrio.
- Algodón.
- Jeringuilla.
Procedimiento:
Se introduce el reactivo biológico bajo una
campana de vidrio en cuyo interior se encuentra
algodón empapado de éter.
Previo a iniciar el experimento se observa
reactividad, respuesta a estímulos y frecuencia
cardiaca
Una vez, bajo la campana se aprecian las
diferentes etapas por las que pasa el animal,
que van desde el estado de incoordinación
hasta la pérdida del conocimiento
con dificultad respiratoria severa y alteraciones
en la frecuencia cardiaca.
Se introduce el reactivo biológico y durante
minutos y se observan los planos de la
anestesia. Al finalizar el animal está inmóvil,
arrefléxico y con pupilas dilatadas.
Resultados: Se aprecian los diferentes planos
de la anestesia general.
Conclusiones: Se nota que los anestésicos
generales son depresores no selectivos del
SNC.
Marcha experimental del sistema nervioso
central
Anticonvulsivantes
Referencia Teórica:
La fenitoína o difenilhidantoína fue sintetizada
en 1908 por Bilz, pero su actividad
anticonvulsivante no fue descubierta hasta
1938. Desde entonces es el fármaco más
utilizado para el tratamiento de las convulsiones,
estando indicada en las crisis tonicoclónicas
generalizadas, crisis parciales,
convulsiones focales y neuralgia del trigémino.
Aunque químicamente esta relacionada
con los barbitúricos, no pertenece a
esa clase de fármacos. La fenitoína tiene
también propiedades antiarrítmicas tipo IB.
- Objetivos: Comprobar que los anticonvulsivantes
previenen las convulsiones
tónico-clónicas.
- Estrategia: Test diagnóstico. Conferencia-
Discusión. Evaluación y Protocolo
Experimental.
- Reactivos Biológicos: Cobayo.
- Reactivos Farmacológico: Difenilhidantona
® Epamin ampolla 5ml 25mg.
Materiales e instrumental:
- Carrete de Ruthenford.
- Electrodos oculares.
- Jaula - Jeringuillas.
- Algodón.
- Alcohol.
Procedimiento:
a) Animal testigo: inducimos convulsiones
tónico-clónicas es el cobayo mediante los
electrodos oculares conectados al carrete
de inducción o de Rutherford. Se determina
el voltaje necesario de menor a mayor.
b) Animal problema nos sirve el mismo co-
MANUAL DE PRÁCTICAS DE FARMACOLOGÍA
258 RECIMUNDO VOL. 4 Nº 1 (2020)
bayo al que administramos Difenilhidantoina
IP a Ds 5 mg/kg. Luego de 10 minutos
aplicamos el voltaje anterior con los electrodos
aculares desde el carrete de inducción.
Resultados:
a) Animal testigo luego de administrar el
voltaje necesario se producen convulsiones
tónico-clónicas en el cobayo.
b) Animal problema luego de inyectarse Difenilhidantoina
y al administrarse el voltaje
anterior y aun elevándolo no se producen
convulsiones en dicho cobayo.
Conclusiones: La Difenilhidantoina previene
las convulsiones tónico-clónicas.
Marcha experimental sistema nervioso central
Neurolépticos
Referencia Teórica:
Los tranquilizantes más fuertes se usan
para los tratamientos de la psicosis y otros
transtornos mentales como la esquizofrenia,
las manías y el deliriun tremens, éste originado
por la abstinencia de bebidas alcohólicas.
Entre los más usados se encuentran
la reserpina, el haloperidol, la butirofenona,
la tioxantina, las fenotiacinas y sus derivados.
Esos fármacos se conocen como neurolépticos,
que provienen de las palabras
griegas neuro ="nervio", y lepto ="atar'.
- Objetivo: Demostrar la acción depresora
sobre el SNC de los tranquilizantes mayores.
- Estrategia: Test diagnóstico. Conferencia-
Discusión. Evaluación y Protocolo
Experimental.
- Reactivo Biológico: Rata Albina.
- Reactivo Farmacológico: Levomepromazina
(R) sinogan 25mg/ ml/ ampollas.
Materiales o instrumental:
- Jaula
- Rejilla de alambre - Balanza.
- Jeringuillas - Cuerda.
Procedimiento:
- Se pesa a la rata. Se calcuola la dosis
total.
- Se administra levomepromazina
Ds=25mg/Kg IP y se contabiliza el
tiempo y sintomatología de depresión
del SNC.
Resultados:
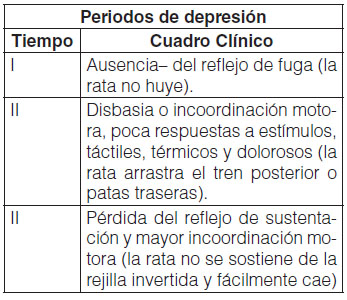
Conclusiones: Se comprueba que los neurolépticos
(levomepromazina) deprime selectivamente
el SNC y en sobredosis puede
producir muerte por inhibición de los centros
vegetativos del bulbo raquídeo, (Periodo
V o muerte de la rata).
Marcha experimental sistema renal
Diuréticos
Referencia Teórica:
Como se acaba de exponer, son ya varias las
familias químicas con capacidad de actuar
en el segmento diluyente del asa de Henle.
Entre todas ellas, las mejor estudiadas y
más utilizadas son los sulfamoilbenzoatos,
cuyo representante más característico es la
furosemida, y los derivados fenoxiacéticos,
especialmente el ácido etacrínico.
Sitio y mecanismo de acción: Son diuréticos
LITUMA PEÑARRETA, O., AVALOS MORENO, E., ZEA MORALES, A., & CASTRO GARCÍA, R.
RECIMUNDO VOL. 4 Nº 1 (2020) 259
que producen una diuresis copiosa y, en
general, de corta duración. Su sitio crítico
de acción es el segmento diluyente medular
y cortical, y concretamente el epitelio de
la porción o segmento grueso de la rama
ascendente del asa de Henle, razón por la
cual frecuentemente son denominados diuréticos
del asa.
Objetivos: Determinar el aumento de la diuresis
o excreción urinaria por furosemida.
Estrategia: Test diagnóstico. Conferencia-
Discusión. Evaluación y Protocolo Experimental.
Reactivos Biológicos: 2 cobayos (de características
semejantes y con buena ingestión
de agua).
Reactivos Farmacológicos:
Furosemida R. lasix ampolla 2ml = 20mg
Ds= 20mg/ K.
Materiales e Instrumental:
- Vaso pirex con medida
- Embudos
- Rejillas - Soportes
- Balanza
- Jeringuillas
Procedimiento:
- Animal problema se le inyecta furosemida
20mg/kg IP y se lo coloca en el embudo
rotulado problema.
- Cobayo testigo se le administra agua
destilada IP en la misma cantidad y se
lo coloca en el embudo respectivo.
- Se contabiliza la diuresis cada 10 minutos.
Conclusiones:
a. El animal problema se incrementa la cantidad
de orina por efecto de la furosemida
que actúa como diurético.
b. Animal testigo tiene una diuresis normal y
menor al cobayo problema.
Marcha experimental sistema cardiovascular
Cardiotónicos
Referencia Teórica:
En pacientes con insuficiencia cardiaca,
la digoxina aumenta la fuerza contráctil y
el volumen minuto, y disminuye la frecuencia
cardiaca, la presión y el volumen telediastólicos
ventriculares, la presión capilar
pulmonar, la tensión parietal y el índice cardiotorácico.
Como consecuencia, mejora
los signos de congestión pulmonar y de
hipoperfusión tisular y aumenta la capacidad
funcional evaluada como tolerancia al
ejercicio. El aumento de la contractilidad y
del volumen minuto aparece tanto en el corazón
normal como en el insuficiente, aunque
es mucho más marcado en este último
y persiste a lo largo del tiempo, lo que indica
que no aparece tolerancia a sus efectos.
Objetivo: Acción de los cardiotónicos sobre
el corazón “in situ” de rana.
Estrategia: Test diagnóstico. Conferencia-
Discusión. Evaluación y Protocolo Experimental.
Reactivo Biológico: Rana.
Reactivo farmacológico: Digoxina.
Materiales e instrumental:
- Tabla operatoria.
- Instrumental de disección quirúrgica.
- Estilete.
- Quimógrafo -Soportes.
- Palanca de Starling.
- Pluma inscriptora.
- Seda quirúrgica.
Procedimiento:
- Se descerebra al animal con un estilete en la región cervical.
- Se fija la rana por sus cuatro extremidades y la tabilla operatoria en decúbito dorsal.
- Se diseca la cavidad toracoabdominal se diseca cuidadosamente el corazón cortando el pericardio.
- Se fija el ápex o punta del corazón con una seda quirúrgica y el otro extremo se une a la palanca de Starling que tiene en su extremo una pluma inscritota que marcara la actividad cardiaca en un quimógrafo.
- Actividad normal por automatismo cardiaco propio.
- Se ponen 1-2-4 gotas de Adrenalina dilución de 1(10)-5 y se grafica.
- Se administra 2 – 4 – 8 gotas de Digoxina en dilucion de 2(10)-4 y se grafica.
Conclusiones:
a) El corazón tiene automatismo propio (trazado
normal).
b) La adrenalina incrementa el trabajo del
corazón. Es estimulante cardiaco (inotropismo
+, cronotropismo + ).
c) Digoxina es cardiotónico ( inotropismo +,
cronotropismo -)
Marcha experimental aparato digestivo
Antihelmínticos.
Referencia Teórica:
Los antihelmínticos son fármacos capaces
de eliminar los nematodos cestodes o trematodes,
parásitos largos que en general
se alojan en órganos y tejidos.
Existen dos tipos de sustancias:
a)Vermicidas: que producen la muerte del helminto.
b)Vermífugos: eliminan el helminto del intestino sin producir su muerte.
Dentro del grupo de antihelmínticos tenemos:
a) Benzoimidazoles = albendazol, tialbendazol.
b) Tetrahidropirimidinas = dietilcarbamicina.
c) Cininas = pirvinio.
d) Hidrocarburos halogenados = tetracloroetileno.
Objetivo: Demostrar la acción vermicida y
vermífuga en la lombriz de tierra.
Estrategia: Test diagnóstico. Conferencia-
Discusión. Evaluación y Protocolo Experimental.
Reactivo biológico: Lombriz de tierra ( 8 –
10 ).
Reactivo Farmacológicos: Sol salina fisiológica
Fco 500 ml.
Albendazol ®Susp 400mg Fco 30ml
Pirerazina ® Susp 2% Fco.
Materiales e instrumental:
- Cajas de Petrie
- Gotero
- Jeringuillas - Algodón
- Alcohol
Procedimiento:
a. Testigo, poner sol. salina fisiológica 30ml
en una cajá de Petrie y se agrega 2 lombrices
de tierra vivas.
b. Problema, poner en una cajá de Petrie
30 ml de Albendazol e introducir 2 vermes.
c. Problema, en una cajá de Petrie poner
30ml de Piperazina e introducir 2 lombrices
de tierra vivas. Luego de 10 minutos lavar
lãs 3 cajas de Petrie con sol salina por 3
veces cada una.
Resultados: Testigo, se mantienen vivos los
vermes de tierra.
b. Problema, las lombrices mueren a pesar
de los lavados y eliminar el medicamento
(acción vermicida).
c. Problema, las lombrices de tierra inmóviles
recobran su vitalidad luego de eliminar
el fármaco con varios lavados (acción vermífuga).
Conclusiones:
a. Testigo, vitalidad normal.
b. Albendazol tiene acción vermicida.
c. Piperazina tiene acción vermífuga pues luego de parálisis flácida el reactivo biológico recobra su vitalidad.
Marcha experimental sistema endocrino
Ocitócicos y útero inhibidores.
Referencia teórica:
La ocitocina estimula la producción de potenciales
espiga en las células miometriales,
aumentando la frecuencia de descarga
y el número de potenciales presentes en
una descarga, así como su amplitud.
Estimulantes 2-adrenérgicos.- Los fármacosempleados son: ritodrina, terbutalina, salbutamol, fenoterol y hexoprenalina.
Acciones farmacológicas.- En el útero grávido,
los estimulantes 2 inhiben la contracción
uterina, tanto la espontánea como la
provocada por diversos estímulos. Por este
motivo, según la dosis, aparecen en la madre
taquicardia, reducción de la presión
diastólica sin modificación de la sistólica y
aumento de la presión diferencial.
Objetivo: Acción de las drogas ocitócicas y
útero inhibidores sobre el útero.
Estrategia: Test diagnóstico. Conferencia-
Discusión. Evaluación y Protocolo Experimental.
Reactivo biológico: cobayo hembra.
Reactivo farmacológico:
Ocitocina ® pitocin ampolla 1ml = 10ul
Fenoferol ® ranote
Materiales e instrumental:
- Equipo de disección quirúrgica
- Oxigeno
- Seda quirúrgico
- Baño Maria
- Quimógrafo
- Soportes
- Palanca de Starling - Pluma inscriptora
- Algodón
- Alcohol
- Caja de Petrie
- Sol salina fisiológica
- Vástago de vidrio
- Sol. Tyrode.
Procedimiento:
Se descerebra al animal mediante traumatismo cervical.
Se diseca la cavidad abdominal y el útero del cobayo hembra.
Se extraen los cuerpos uterinos y se los coloca en baño de María brindándole las mismas condiciones que el organismo vivo:
A/Temperatura 37°C con baño María y comprobar temperatura. B/Oxigenación constante, mediante un vástago de oxígeno. C/Medio interno con sol. Tyrode semejante al medio fisiológico de la cavidad abdominal.
El extremo de cuerno uterino va unido con seda quirúrgica al vástago de vidrio que da la oxigenación permanente.
El otro extremo va conectada con una seda quirúrgica a la palanca de Starling que tiene en un extremo la pluma inscriptora que marca la actividad muscular en un quimógrafo.
Se grafica cada 2 minutos y se realizan lavados sucesivos
Trazado normal
Ocitocina 0.1ml se lava
4’ ocitocina 0.1 ml se lava 6’ fenoterol 0.1 lavado
8’ ocitocina + orciprenalina
Resultado y Gráficos:
a) Trazado normal, el útero tiene contracciones en gestación.
b) Útero estimulación los ocitocina aumenta la altura y el número de espigas o contracciones.
c) Mayor estimulación uterina.
d) Útero inhibición, el fenoterol disminuye el número de contracciones y la fuera de contracción.
e) Estimulación + inhibición, aumenta y cae la curva o contracción uterina.
Conclusiones: En el útero grávido la ocitocina actúa como estimulante de las contracciones uterinas y el fenoterol actúa como útero inhibidor.
Marcha experimental sistema respiratorio
Histamina y antihistamínicos
Referencia Teórica:
La histamina es una amina sintetizada en 1907, que posteriormente fue aislada en los tejidos. Está compuesta por un anillo imidazólico y una cadena lateral etilamino. Se encuentra almacenada principalmente en los mastocitos del tejido conjuntivo y en las células basófilas de la sangre.
Objetivo: Acción de la histamina y antihistamínicos sobre el sistema respiratorio.
Estrategia: Test diagnóstico. Conferencia-Discusión. Evaluación y Protocolo Experimental.
Reactivo biológico: 3 Cobayos.
Reactivos Farmacológicos:
Histamina Amp
Diefenhidramina Amp
Dexametasona Amp
Materiales e instrumental:
- Cámara de nebulización
- Jaula
- Jeringuillas - Algodón
- Alcohol
- Oxígeno
Procedimiento:
a) Cobayo testigo, se lo coloca en la cámara la de nebulización a una atmósfera de Histamina 1(10)-3, que se nebuliza con una corriente continua de oxígeno y se observa el cuadro clínico asmatiforme que se presenta en el animal. Luego se le administra Salbutamol IP 1 amp.
b) Cobayo problema, se lo introduce en la cámara de nebulización con una atmósfera de Histamina + Dexametasona IP 1 amp.
c) Otro cobayo problema se le administra Histamina en la cámara de nebulización + Difenhidramina IP 1 amp.
Resultados:
a) Testigo, antagonismo no competitivo pues se produce crisis asmática por Histamina en el cobayo (disnea, tos, tiraje intercostal, aleteo nasal, estridor). El mismo que se elimina con Salbutamol que es broncodilatador.
b) Problema, antagonismo no competitivo pues se produce crisis asmática en el cobayo inducida por histamina la que se elimina con corticoides como Dexametasona.
c) Problema, antagonismo competitivo pues el antihistamínico como la Difenhidramina bloquea los receptores por concentración e impide que la Histamina produzca crisis asmática en el cobayo.
Conclusiones:
- La histamina es un potente broncocotrictor y actúa desencaminado crisis asmática.
- Salbutamol es un broncodilatador que elimina las crisis asmáticas.
- Dexametasona y los corticoides mejoran la crisis asmática al disminuir el edema de la mucosa respiratoria.
- El antihistamínico Loratadina por gradiente de concentración evita que la histamina desencadene crisis asmática.
Marcha experimental aparato digestivo
Sinergismo y antagonismo medicamentoso.
Referencia teórica:
La acetilcolina (ACh) es el neurotransmisor específico en las sinapsis del sistema nervioso somático (SNS) y en las sinapsis ganglionares del sistema nervioso autónomo (SNA), así como en los órganos diana de la división parasimpática (ver Ruta 11). La acetilcolina se encuentra también ampliamente distribuida en el encéfalo y es un neurotransmisor clave en la regulación de los niveles de vigilancia y en el funcionamiento de grandes áreas de asociación.
Objetivos: Comprobar el sinergismo y antagonismo en ileon terminal, “in vivo”.
Estrategia: Test diagnóstico. Conferencia-Discusión. Evaluación y Protocolo Experimental.
Reactivo biológico: Rata albina.
Reactivos farmacológicos:
Acetilcolina sol 0.002% dosis 0.5 – 1 – 2 ml
Neostagmine ® Prostigmine sol 0.001% amp 0.5mg = 1ml
Atropina sulfato sol 0.1% dosis 0.1mg 1ml
Solución tyrode.
Materiales e instrumental:
- Baño María
- Seda quirúrgica
- Caja de Petrie
- Equipo de disección quirúrgica
- Palanca de Starling - Termómetro
- Pluma inscriptora
- Quimógrafo
- Soportes
Procedimiento:
Descerebramos el cobayo mediante técnica de Magnus.
Disecamos la cavidad abdominal y seccionamos 3 – 6cm de ileon Terminal.
Se une el extremo con seda quirúrgica al vástago de vidrio que da oxigenación constante y el otro extremo va unido a una palanca de Starling que tiene es su extremo una pluma inscriptora para marcar el peristaltismo del intestino en el quimógrafo.
El ileon se mantiene “In vivo” puesto que requiere:
1/ Temperatura 37°C suministrado por el baño Maria. 2/ Oxigenación continua dada por el vástago de vidrio unida a un tanque de oxígeno. 3/ Sol tyrode o fisiológica semejante a la de la cavidad abdominal de la rata.
Se obtiene un trazado normal por el peristaltismo del intestino.
Sinergismo medicamentoso, se administra Acetilcolina 1 -2 – 4 mg + Neostigmine 0.5mg 1 amp.
Antagonismo, Acetilcolina 4mg + Atropina 0.5 mg 1 amp.
Se lava la preparación varias veces luego de cada paso experimental.
Resultados y gráficos:
a) Trazado normal del peristaltismo.
b) Sinergismo medicamentoso entre la Aceticolina + Neostigmine con mucha elevación de la contracción muscular y de la curva.
c) Antagonismo medicamentoso con caída de la curva y de la contracción por administración de Acetilcolina + Atropina.
Conclusiones:
a) Sinergismo o aumento de la acción farmacológica por unión de las drogas colinérgicas Aceticolina mas Neostigmine.
b) Antagonismo o disminución de la acción farmacológica entre Acetil colina mas Atropina, esta última es anticolinérgica.
Marcha experimental de toxicologi
Intoxicación por organofosforados.
Referencia Teórica:
Derivan de la propiedad fundamental de inhibir la inactivación de la acetilcolina en los sitios donde ésta se libere fisiológicamente, tanto en el SNC como en las terminaciones nerviosas periféricas, somáticas o vegetativas, pudiendo, por lo tanto, producir los siguientes efectos: a)estimulación de los receptores muscarínicos en los órganos efectores vegetativos; b) estimulación, seguida de depresión o parálisis, de todos los ganglios vegetativos y de la musculatura esquelética por activación nicotínica; c) estimulación con depresión posterior ocasional, de receptores colinérgicos centrales. Su acción, por lo tanto, es de carácter colinérgico, pero resulta afectada por algunos factores: a) la capacidad de los compuestos para atravesar membranas: fisostigmina y órgano fosforados no poseen N cuaternario, por lo que se absorben con facilidad, atraviesan la barrera hematoencefálica y ejercen efectos en el SNC, mientras que la neostigmina y el edrofonio no lo hacen y b) la capacidad de activar directamente receptores nicotínicos, tanto en ganglios como en órganos efectores (p. ej., placa motriz del músculo esquelético).
Objetivo: Demostrar la acción farmacológica (tóxica) del órgano fosforado en el ratón y su tratamiento.
Estrategia: Test diagnóstico. Conferencia-Discusión. Evaluación y Protocolo Experimental.
Reactivo Biológico: 2 lauchas.
Reactivo Farmacológico:
- Paranitrofenildietiltiofosfato (R) Baygon sol 3% en alcohol etílico
- Atropina (R) atropina sol 1%
- Sol. Salina 0.9%.
Materiales e Instrumental:
- Jaulas
- Jeringuillas
- Rejillas
Procedimento:
a) Animal testigo, se administra ranitrofenildietiltiofosfato 0.1ml IP luego se determina el período de latencia hasta la producción de síntomas de toxicidad.
b) Animal problema, dministramos IP paranitrofenildietiltiofosfato 0.1 ml + atropina Ds 25mg/ kg IP , se espera el período de latencia y la sintomatología.
Resultados:
a) Animal testigo: Presenta síntomas nicotínicos como temblor, rigidez, fasciculaciones, hipersensibilidad; síntomas muscarínicos como miosis, salivación, dificultad respiratoria, relajación de esfínteres, llegando a la muerte del animal.
b) Animal problema: No se presentan síntomas y si hay manifestaciones tóxicas se administra más atropina así el animal no muere.
Conclusiones:
El órganofosforado paranitrofenildietiltiofosfato produce intoxicación con síntomas parasimpáticos o colinérgicos (animal testigo) los que se inhiben o eliminan con atropina (anticolinérgico o parasimpaticolitico). Es decir se produce un antidotismo competitivo en el animal problema.
Bibliografía
AVILES, C. (2004). Gestión de Recursos Humanos. Quito: Editorial Universidad Central.
Chéry, P. M. (2010). farmacología básica y clínica. México: McGRAW-HILL INTERAMERICANA EDITORES, S.A. Obtenido de www.rinconmedico.smffy.com
DELGADO, E. (2002). Evaluación de Proyectos. Quito: Asociación de Facultades Ecuatorianas de Filosofía, Letras y Ciencias de la Educación.
Fernández, P. L., Moreno González, A., Leza Cerro, J. C., Lizasoain Hernández, I., Moro Sánchez, M. Á., & Portolés Pérez, A. (2009). Velázquez. Farmacología Básica y Clínica (18 ed.). Editorial Médica Panaméricana. Obtenido de https://books.google.co.ve/books/about/Vel%C3%A1zquez_Farmacolog%C3%ADa_B%C3%A1sica_y_Cl%C3%ADn.html?id=BeQ
6D40wTPQC&printsec=frontcover&source=kp_read_button&redir_esc=y#v=onepage&q&f=false
FLÓREZ, J. (2016). Pasión por la Farmacología Humana. Generación Elsevier.
FRAGA, C. H. (1997). Modelación del Proceso de formación de Profesionales. Cuba: ISPETP.
Hilal-Dandan, Randa ; Brunton, Laurence. (2013). Goodman & Gilman. MANUAL DE FARMACOLOGÍA Y TERAPÉUTICA (2da Edicion ed.). California: McGRAW-HILL INTERAMERICANA EDITORES, S. A.
SCH, E. (2005). Evaluación y los escenarios sociopolíticos a inicios del tercer milenio. quito: Universidad Central del Ecuador.
Litter, M. (1983). Farmacología. Madrid-España: El Ateneo.
LOZADA, B. (2004). Teoría y Diseño Curricular. Quito: Editorial Universidad Central.
Malgor, L. A., & Valsecia, M. E. (2000). Capítulo 2. Farmacología general: Farmacocinética. Obtenido de Malgor LA, Valsecia ME. Farmacología Médica. 2da ed. (p. 13-32).: http://med.unne.edu.ar/farmaco.html
Meyer, H. H. (1924). La Farmacología experimental como base del tratamiento médico. Tratado para uso de médicos y estudiantes. Editorial Saturnino Callej.
MONTENEGRO, C. C. (2005). Formulación y Evaluación de Proyectos Quito Universidad Central del Ecuador.
MONTENEGRO, M. (2003-2005). Proyecto de Evaluación Intitucional. Quito: Universidad del Norte.
PACHECO, O. (2005). Proyectos Educativos Guayaquil. Guayaquil: Editorial Miinerva.
PORTO, A. (1997). Apuntes para el Estudio de Medios en Tecnología Educativa. Habana-Cuba: Editorial ISPETP.
YEPEZ, TERAN, ALEGRÍA. (2004). Planificación Estratégica. Quito: Editorial Universidad Central.

Reconocimiento-NoComercial-CompartirIgual
CC BY-NC-SA
Esta licencia permite a otros entremezclar, ajustar y construir a partir de su obra con fines no comerciales, siempre y cuando le reconozca la autoría y sus nuevas creaciones estén bajo una licencia con los mismos términos.





