INTRODUCCIÓN
La cardiopatía isquémica es la principal causa
de muerte y la pérdida de calidad de todo
el mundo la vida (Vedanthan, Seligman, &
Fuster, 2014). En Brasil, se estima que esta
relacionado con una tasa anual de aproximadamente
55 muertes por cada 100.000
habitantes (Piegas, Avezum, & Guimarães,
2013). El síndrome coronario agudo (SCA),
con su amplia gama de manifestaciones, adquiere
un papel principal en estas estadísticas,
y la revascularización miocárdica procedimientos
y farmacoterapia antitrombótico
son pilares fundamentales de su tratamiento.
La hemostasia es un proceso fisiológico
mantenido a través de una compleja interacción
entre factores endotelio, plaquetas
y de la coagulación. En condiciones de
emergencia y el desequilibrio, la hemostasia
puede conducir a la formación de trombos
arteriales o venosas, lo que resulta en la
aparición de episodios coronarios agudos,
eventos cerebrovasculares, o episodios de
tromboembolismo. En este contexto, y junto
con la terapia anticoagulante, antiplaquetas
drogas se destacan en la gestión de estas
condiciones.
Las situaciones que implican lesión y la interrupción
del revestimiento endotelial estimulan
proteínas plaquetarias adhesión a
subendotelial matriz. Esta interacción activa
señales intracelulares que promueven
la liberación de adenosina difosfato (ADP),
adrenalina, serotonina, trombina y tromboxano
A2, potentes agonistas de la activación
plaquetaria. Una vez que las plaquetas se
activan, la glicoproteína IIb-IIIa complejos se
unen al fibrinógeno para constituir la etapa final
de la agregación plaquetaria y formación
de trombos (Fuster & Sweeny, 2011)
Los factores que activan este proceso y los
receptores implicados en ella se han convertido
en objetivos para el desarrollo de
agentes antitrombóticos. Evidencia basada
en medicina permitido a la llegada, la implementación
y el perfeccionamiento del
enfoque terapéutico actual. Sin embargo,
mediante el aumento de la esperanza de
vida de la población y la coexistencia de
múltiples comorbilidades, que a menudo se
encuentran escenarios clínicos en el que el
riesgo de complicaciones isquémicas va de
la mano con el riesgo de complicaciones
hemorrágicas. Esto exige un conocimiento
completo del arsenal de agentes antiplaquetarios
en cuanto a su indicación, dosis y momento
de la administración.
El objetivo de esta revisión es definir el papel
de antiagregantes plaquetarios en la gestión
de ACS, volviendo a visitar los aspectos que
han sido ya consolidados y que abordan temas
de actualidad y todavía controvertidos
sobre el tema.
Metodología
Para el desarrollo de este proceso investigativo,
se plantea como metodología la encaminada
hacia una orientación científica particular
que se encuentra determinada por la
necesidad de indagar en forma precisa y coherente
una situación, en tal sentido (Davila,
2015) define la metodología “como aquellos
pasos previos que son seleccionados por el
investigador para lograr resultados favorables
que le ayuden a plantear nuevas ideas”.
(p.66)
Lo citado por el autor, lleva a entender que
el desarrollo de la acción investigativa busca
simplemente coordinar acciones enmarcadas
en una revisión bibliográfica con el fin de
complementar ideas previas relacionadas al
tratamiento antiplaquetario en el síndrome
coronario agudo a través de una revisión
de literatura, para así finalmente elaborar un
cuerpo de consideraciones generales que
ayuden a ampliar el interés propuesto.
Tipo de Investigación
Dentro de toda práctica investigativa, se
precisan acciones de carácter metodológico
mediante las cuales, se logra conocer y proyectar los eventos posibles que la determinan,
así como las características que hacen
del acto científico un proceso interactivo
ajustado a una realidad posible de ser interpretada.
En este sentido, se puede decir,
que la presente investigación corresponde al
tipo documental, definido por Castro (2016),
“se ocupa del estudio de problemas planteados
a nivel teórico, la información requerida
para abordarlos se encuentra básicamente
en materiales impresos, audiovisuales y /o
electrónicos”. (p.41).
En consideración a esta definición, la orientación
metodológica permitió la oportunidad
de cumplir con una serie de actividades inherentes
a la revisión y lectura de diversos
documentos donde se encontraron ideas
explicitas relacionadas con los tópicos encargados
de identificar a cada característica
insertada en el estudio. Por lo tanto, se realizaron
continuas interpretaciones con el claro
propósito de revisar aquellas apreciaciones
o investigaciones propuestas por diferentes
investigadores relacionadas con el tema de
interés, para luego dar la respectiva argumentación
a los planteamientos, en función
a las necesidades encontradas en la indagación.
Fuentes Documentales
El análisis correspondiente a las características
que predomina en el tema seleccionado,
llevan a incluir diferentes fuentes documentales
encargadas de darle el respectivo apoyo
y en ese sentido cumplir con la valoración
de los hechos a fin de generar nuevos criterios
que sirven de referencia a otros procesos
investigativos. Para (CASTRO, 2016)
las fuentes documentales incorporadas en
la investigación documental o bibliográfica,
“representa la suma de materiales sistemáticos
que son revisados en forma rigurosa
y profunda para llegar a un análisis del fenómeno”.(
p.41). Por lo tanto, se procedió
a cumplir con la realización de una lectura
previa determinada para encontrar aquellos
aspectos estrechamente vinculados con el tema, con el fin de explicar mediante un desarrollo
las respectivas apreciaciones generales
de importancia.
Técnicas para la Recolección de la Información
La conducción de la investigación para ser
realizada en función a las particularidades
que determinan a los estudios documentales,
tiene como fin el desarrollo de un conjunto
de acciones encargadas de llevar a la
selección de técnicas estrechamente vinculadas
con las características del estudio.
En tal sentido, (Bolívar, 2015), refiere, que es
“una técnica particular para aportar ayuda a
los procedimientos de selección de las ideas
primarias y secundarias”. (p. 71).
Por ello, se procedió a la utilización del subrayado,
resúmenes, fichaje, como parte básica
para la revisión y selección de los documentos
que presentan el contenido teórico.
Es decir, que mediante la aplicación de estas
técnicas se pudo llegar a recoger informaciones
en cuanto a la revisión bibliográfica
de los diversos elementos encargados
de orientar el proceso de investigación. Tal
como lo expresa, (Bolívar, 2015) “las técnicas
documentales proporcionan las herramientas
esenciales y determinantes para
responder a los objetivos formulados y llegar
a resultados efectivos” (p. 58). Es decir, para
responder con eficiencia a las necesidades
investigativas, se introdujeron como técnica
de recolección el método inductivo, que hizo
posible llevar a cabo una valoración de los
hechos de forma particular para llegar a la
explicación desde una visión general.
Asimismo, se emplearon las técnicas de
análisis de información para la realización
de la investigación que fue ejecutada bajo
la dinámica de aplicar diversos elementos
encargados de determinar el camino a recorrer
por el estudio, según, (Bolívar, 2015) las
técnicas de procesamiento de datos en los
estudios documentales “son las encargadas
de ofrecer al investigador la visión o pasos que debe cumplir durante su ejercicio, cada
una de ellas debe estar en correspondencia
con el nivel a emplear” (p. 123). Esto indica,
que para llevar a cabo el procesamiento de
los datos obtenidos una vez aplicado las técnicas
seleccionadas, tales como: fichas de
resumen, textual, registros descriptivos entre
otros, los mismos se deben ajustar al nivel
que ha sido seleccionado.
Resultados
a) El ácido acetilsalicílico
El ácido acetilsalicílico (ASA) a dosis bajas
ciclooxigenasa selectivamente inhibe (COX)
-1, el establecimiento de la actividad antiplaquetaria,
mientras que a altas dosis que
inhibe la COX-1 y COX-2 con efectos anti-inflamatorios
y analgésicos.
Este medicamento se absorbe rápidamente,
alcanzando una concentración máxima en
plasma 30 minutos después de la ingesta,
en el caso de una formulación regular, y 4
horas después de la ingesta, en el caso de
una formulación de liberación entérica (Patrono,
Baigent, Hirsh, & Roth, 2008)
Dado que los efectos secundarios gastrointestinales
de aumento ASA en proporción a
su dosis, una dosis de carga oral de 150325 mg (tragado, si una formulación regular,
y masticó, si un uno enteral) se recomienda
para ACS, o 80-150 mg por vía intravenosa
en lugares en los que esta presentación está
disponible, seguido de 81-100 mg como de
mantenimiento. En el estudio pionero Segundo
Estudio Internacional de Supervivencia
del infarto (ISIS) -2, ASA promovido un significativo
23% de reducción en cardiovascular
la mortalidad en comparación con placebo
después de 5 semanas de tratamiento en
pacientes con infarto agudo de miocardio
(IAM) con elevación del segmento ST, con
este efecto ser aditivo y sinérgico cuando
se asocia con estreptoquinasa, la reducción
de la tasa de eventos en un 42% (ISIS-2 (Second
International Study of Infarct Survival) , 1988) Estas beneficios fueron corroborados
por varios estudios posteriores y por la compilación
de sus datos en grandes meta-análisis,
convirtiéndose así en uno de los pilares
de la farmacoterapia antitrombótico en los
diferentes espectros de ACS.
Las situaciones que constituyen una contraindicación
clara para ASA son raras, y
incluyen sangrado digestivo principalmente
activa y hipersensibilidad conocida (urticaria,
broncoespasmo, o anafilaxia), aunque
diferentes protocolos de desensibilización
se han descrito lo que permite el uso crónico
de estos medicamentos con eficacia y seguridad
demostrada.
B) P2Y12 receptor plaquetario antagonistas
La asociación entre ASA y una P2Y12 antagonista
del receptor, conocida como terapia
antiplaquetaria dual, es la base del tratamiento
de los pacientes con SCA y los sometidos
a intervención coronaria percutánea
(PCI). La ticlopidina es una primera generación
de tienopiridina derivado que, a pesar
de su eficacia y debido a su hematológica
(trombocitopenia, anemia aplástica, la púrpura
trombocitopénica trombótica, neutropenia)
y los efectos secundarios gastrointestinales,
ha sido reemplazado rápidamente por
clopidogrel (Steinhubl, Tan, Foody, & Topol,
2009).
b.1) Clopidogrel
El clopidogrel es un agente de tienopiridina
que forma irreversible bloquea el P2Y12 receptor.
La inhibición de estado estacionario
de la función plaquetaria con clopidogrel se
consigue con una dosis de mantenimiento
de 75 mg después de 5-7 días desde el inicio
del tratamiento, mientras que con la administración
de 300 mg y 600 mg de dosis
de carga, este efecto se alcanza en 6 y 2 horas,
respectivamente, un aspecto relevante
en el contexto de las emergencias médicas.
En el ensayo clínico de referencia clopidogrel
en angina inestable para prevenir recurrentes
Eventos (curación), 12.562 pacientes
con sin elevación del ST IAM tratados con
AAS fueron aleatorizados para recibir clopidogrel
o placebo durante 3 a 12 meses
(Yusuf, y otros, 2001) El grupo clopidogrel
exhibió una reducción significativa del 20%
en el riesgo de enfermedades cardiovasculares
muerte, preinfarto o accidente cerebrovascular
en comparación con el grupo
de placebo, con beneficios ya aparentes en
las primeras horas después de la iniciación
de la terapia e independiente de la estratificación
invasiva. En el escenario de IAM
con elevación del segmento ST, dos importantes
estudios validados clopidogrel como
una terapia adyuvante eficaz. Entre 3.491
pacientes asignados al azar a 300 mg de
clopidogrel y 75 mg de clopidogrel mantenimiento
versus placebo en el ensayo clínico
de clopidogrel como adyuvante Terapia de
reperfusión-Trombolisis en el Infarto de Miocardio
(CLARITY-TIMI), de los cuales 28%
fueron sometidos a trombólisis, se observó
99.7 una reducción del 36% en el riesgo de
muerte, recurrente AMI, o ocluida la arteria
del infarto relacionada en el momento de la
angiografía (Sabatine, y otros, 2005). Por el
contrario, en el estudio, Clopidogrel y Metoprolol
en el Infarto de Miocardio Trial (COMMIT),
entre 45.852 pacientes asignados al
azar, con 50% de someterse a la trombólisis,
la administración de una dosis diaria de 75
mg de clopidogrel durante un período medio
de 28 días resultó en un 9 % de reducción
en las tasas de muerte, reinfarto o accidente
cerebrovascular en comparación con el placebo
(Chen, y otros, 2015).
Por lo tanto, el apoyo de los resultados de
ensayos controlados aleatorios en ACS y
por las características farmacodinámicas y
farmacocinéticas de clopidogrel, se recomienda
una dosis de carga de 600 mg para
los pacientes en quien la estratificación del
riesgo invasivo o que se predice son remitidos
para la ICP primaria, y 300 mg para
pacientes se somete a terapia fibrinolítica. Una excepción debe hacerse a pacientes
con antecedentes de trombólisis que son de
edad ≥ 75 años, en los que la dosis de carga
debe ser omitido. En ausencia de un claro
beneficio del mantenimiento de clopidogrel
en una dosis doble (150 mg), la dosis debe
ser de 75 mg.
Sin embargo, clopidogrel presenta limitaciones
y las necesidades no satisfechas,
explica en parte por sus propiedades, tales
como lento inicio y la retirada y el potencial
de inhibición plaquetaria limitado. La variabilidad
interindividual de la acción del fármaco
es grande, con el porcentaje de pacientes
que muestran inadecuada respuesta
terapéutica estimada en hasta un 35%. Los
mecanismos involucrados son multifactoriales
e incluyen interacciones de drogas (p.ej,
inhibidores de la bomba de protones tales
como omeprazol y esomeprazol), el medio
ambiente y comorbilidades clínicos (p.ej, La
adherencia a la terapia, tabaquismo, diabetes
mellitus, obesidad, ACS), además de los
polimorfismos genéticos, con énfasis en los
alelos que determinan una pérdida de función
CYP2C19.18 Se sabe que los pacientes
con estas variantes están en mayor riesgo
de trombosis del stent, la recurrencia de
IAM y muerte (Holmes & Dehmer, 2010) Sin
embargo, aunque el tema sigue siendo objeto
de escrutinio en los estudios en curso, la
evidencia actualmente disponible no respalda
la individualización de la terapia basada
en los resultados de las pruebas genéticas
o la medición de la función plaquetaria. Con
eso, un vasto campo de la investigación se
ha abierto con un tratamiento diferente propuestas,
nuevo P2Y12 antagonistas de los
receptores, y el bloqueo de nuevas dianas
en la superficie de las plaquetas.
b.2) Prasugrel
Similar a clopidogrel, prasugrel es una tienopiridina
de segunda generación que es
un profármaco y requiere biotransformación
para convertirse en un metabolito activo. Sin
embargo, tiene un inicio más temprano de la acción, a unos 30 minutos después de la
administración de una dosis de carga de 60
mg, además de una respuesta más predecible,
debido a su amplia absorción, una necesidad
de una única etapa de oxidación mediado
por CYP3A4 y CYP2B6, conferir una
mayor biodisponibilidad, mayores niveles de
inhibición de las plaquetas, y menos variabilidad
de la respuesta entre los pacientes.
En el ensayo para evaluar la mejoría en resultados
terapéuticos mediante la optimización
de plaquetas La inhibición con Prasugrel
(TRITON) -TIMI 38 ensayo clínico, 13.608 pacientes
ingresados por SCA con o sin elevación
del segmento ST sometidos a ICP fueron
aleatorizados para recibir una dosis de
carga de 60 mg de prasugrel y 10 mg dosis
de mantenimiento, o una dosis de carga de
300 mg de clopidogrel y 75 dosis de mantenimiento
mg hasta por 15 meses (Wiviott,
Braunwald, & McCabe, 2007). En el tratamiento
Prasugrel se demostró que era superior
con una reducción significativa del 19%
en el riesgo de enfermedades cardiovasculares
muerte, IAM o ictus no mortal, con una
reducción del infarto de 24% y trombosis del
stent de 52%, con una beneficio aún mayor
entre los pacientes con diabetes.
En consonancia con el aumento de la potencia
de antiplaquetario prasugrel, el estudio
encontró un aumento significativo del 32%
en el riesgo de hemorragia grave, incluso
mortal y la vida hemorragia mortal. En los
perfiles de algunos pacientes, la red beneficio
clínico, que considera la eficacia anti-isquémica
y la seguridad, era desfavorable
para prasugrel, incluyendo pacientes con un
ictus previo o ataque isquémico transitorio
(TIA), con edades ≥ 75 años, y con un peso
corporal <60 kg. En las dos últimas situaciones,
en caso de que haya una necesidad de
prescribir el fármaco y una falta de alternativas
terapéuticas, una dosis de mantenimiento
de 5 mg se recomienda. No hay indicios
hasta la fecha en cuanto a la prescripción de
prasugrel para pacientes con SCA que no se
someten a ICP, o en un marco de tiempo que
no sea después de que el conocimiento de la anatomía coronaria y la realización del procedimiento
de intervención. En los pacientes
con una indicación de cirugía de revascularización
miocárdica, prasugrel idealmente
debe interrumpirse durante 7 días.
b.3) Ticagrelor
La representante primera clínicamente disponible
de la clase ciclopentiltriazolopirimidina,
ticagrelor es un P2Y reversible12antagonista
de los receptores, ejerciendo su efecto
inhibidor a través de una unión no covalente
a un sitio de unión de plaquetas diferente de
ADP. A diferencia de la tienopiridina agentes,
ticagrelor no es un profármaco y actúa inmediatamente
después de la absorción oral.
Exhibe, por lo tanto, un rápido inicio de la
acción después de la ingestión de una dosis
de carga de 180 mg y un pico de acción en
2 horas. Con una vida media de plasma de
8-12 horas, ticagrelor requiere una dosis de
mantenimiento de 90 mg cada 12 horas, y
debido a que se une al receptor de una manera
reversible, que tiene una terminación
más temprana de la acción, alrededor de
2-3 días, a pesar de que el prospecto recomienda
su suspensión durante 5 días antes
de una intervención quirúrgica. Dado que
el metabolismo de ticagrelor está mediado
por CYP3A4 o CYP3A45, la administración
concomitante de inductores o inhibidores
del CYP3A4 fuerte durante su uso debe ser
evitado (Bonello, Laine, Kipson, & Mancini,
2014).
En el ensayo clínico de plaquetas La inhibición
y los resultados del paciente (Platón),
18.624 pacientes que ofrecen todas las manifestaciones
de ACS (con la excepción de
aquellos con IAM con elevación del segmento
ST que la trombolisis se sometieron
a) fueron aleatorizados para recibir ticagrelor
o clopidogrel durante 12 meses (Wallentin,
Becker, & Budaj, 2009). En el grupo de ticagrelor,
hubo una disminución significativa
reducción del 16% en el riesgo de muerte
cardiovascular, IAM o carrera. En un preespecificado
análisis jerárquico, ticagrelorsola
redujo la ocurrencia de muerte cardiovascular (21%), AMI (16%), y la trombosis definitiva
stent (33%), sin diferencia en la tasa
de hemorragia grave o mortal. A pesar de
la consistencia de los resultados obtenidos
entre los diferentes subgrupos analizados,
hubo una interacción entre los pacientes
tratados en América del Norte y el resto del
mundo, sin un claro beneficio de ticagrelor
en el primer grupo.
El uso de altas dosis de mantenimiento de
ASA (≥ 200 mg) se cree que es una justificación
probable para este hallazgo, lo que
provocó una alerta para la prescripción de
dosis <200 mg en el uso crónico.
El ticagrelor exhibe efectos pleiotrópicos no
mediadas por su bloqueo de la P2Y12 receptor,
incluyendo la inhibición de la captación
de adenosina por los eritrocitos, lo que
aumenta los niveles circulantes de adenosina.
La adenosina es conocida por tener varias
propiedades, incluyendo la vasodilatación
coronaria, la reducción de la isquemia
y lesión por reperfusión, la inhibición de las respuestas inflamatorias a condiciones de
estrés, cronotrópico negativo y el efecto dromotropo,
la reducción de glomerular la tasa
de filtración, y la estimulación de las fibras
vágales C en el livianos. Estos efectos están
todavía bajo investigación y justificarían, entre
los usuarios de ticagrelor, una mayor prevalencia
de disnea y sin alteración del pulmonar.
Las pruebas de función, hace una pausa
ventricular sin impacto clínico o requisito de
un marcapasos definitivo, elevado de creatinina
en suero y niveles de ácido úrico, así
como una mayor estabilidad eléctrica y una
reducción de las muertes súbitas arrítmicos,
este último todavía en la especulación.
La Tabla 1 proporciona una recopilación de
las principales indicaciones, dosis y recomendaciones
con respecto a la prescripción
de P2Y12 antagonistas de los receptores en
SCA.
Tabla 1. Indicaciones de los antagonistas del receptor P2Y12 en síndromes coronarios agudos
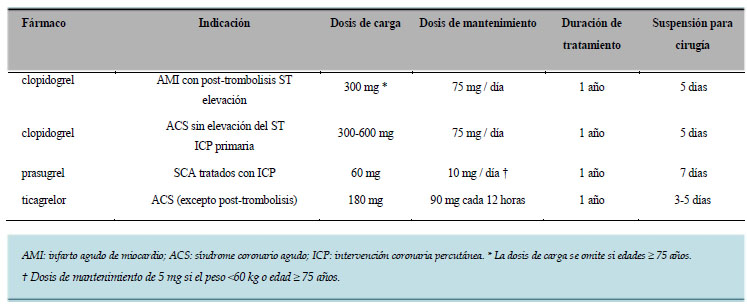
Fuente: Los Autores 2020
Tabla 2. ropiedades farmacológicas de inhibidores de la glucoproteína Iib-IIIa
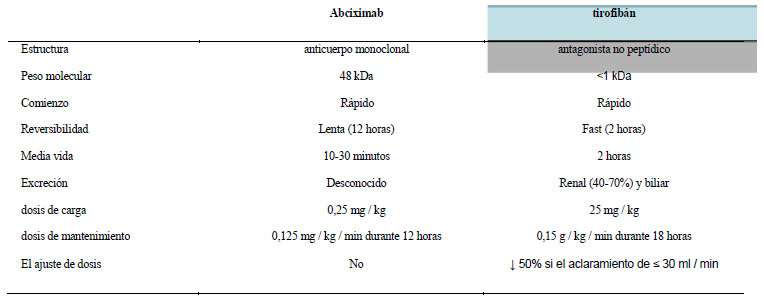
Fuente: Los Autores 2020
c) Inhibidores de la glucoproteína IIb-IIIa
Los inhibidores de la glicoproteína IIb-IIIa
aprobados para uso clínico abciximab,
tirofibán y eptifibatida – son antagonistas
plaquetarios potentes de administración
parenteral, de los cuales sólo los dos primeros
son disponibles comercialmente en
Brasil. Las características farmacológicas
de estos agentes se resumen en la Tabla 2.
Abciximab es un anticuerpo monoclonal
con una alta afinidad para la glicoproteína
receptores IIb-IIIa. Después de una dosis
de carga de 0,25 mg / kg, más del 80% de
los receptores están bloqueados, con una
reducción de la agregación plaquetaria en
respuesta a la estimulación ADP a menos
del 20% del valor de línea de base. Esta inhibición
es mantenido por una infusión continua
de abciximab a una dosis de 0,125 mg
/ kg / min, hasta un máximo de 10 g / min.
La trombocitopenia se informa en el 1-4%
de los pacientes tratados con el fármaco,
comúnmente detectado dentro de las primeras
24 horas y hasta 2 horas después de
la iniciación de su administración. Esto se
cree que es una complicación mediada por
anticuerpos, con una inversión en la mayoría
de los casos después de su suspensión y un requisito ocasional de transfusión de
plaquetas (Moussa & Bennet, 2006)
Tirofibán es un derivado de tirosina no péptido
que actúa a través de un bloqueo reversible
y selectiva del receptor IIb-IIIa de glicoproteína,
evitando su unión a fibrinógeno
y el factor de von Willebrand. Con la excreción
renal y biliar, tirofiban tiene una media
de plasma vida de 1.5-2 horas, con el requisito
de un ajuste de dosis en pacientes con
insuficiencia renal y creatinina aclaramiento
de ≤ 30 ml / min, pero no en los casos de
enfermedad hepática. Cuando se administra
a una dosis de carga de 25 mg / kg, tirofibán
exhibe una eficacia similar a la de
abciximab. Los casos de trombocitopenia
grave, aunque poco frecuente y reversible,
también se han reportado. La aparición de
trombocitopenia grave se atribuye a un mediado
inmune fenómeno, ya que la unión de
tirofibán promueve un cambio conformacional
en el receptor, con la generación de anticuerpos
contra el nuevo epítopo expuesto.
La evidencia de que se ha validado el uso
de inhibidores de la glucoproteína (GPI)
IIb-IIIa en la ICP, dada la capacidad de estos
agentes para reducir periprocedimental
IAM y la necesidad de revascularización urgente, se originó principalmente de estudios
clínicos realizados antes de la llegada
de la tienopiridina agentes y la implantación
del stent rutina. En la era moderna de la cardiología
intervencionista, los meta-análisis
se han realizado estudios para evaluar el
papel real que desempeñan estos agentes
como terapia adyuvante para el PCI.
En el tratamiento de la no elevación del ST
ACS, un meta-análisis que implica 31,402
pacientes demostró una leve pero un beneficio
significativo en la reducción de muertes
y IAM a los 30 días, favoreciendo el uso
de inhibidores de la glucoproteína IIb-IIIa,
especialmente entre los pacientes considerados
de alto riesgo (p.ej, Los pacientes
con marcadores de necrosis miocárdica
positivos, aumento de la carga trombótica,
o lesiones complejas). Un metaanálisis que
participan siete ensayos aleatorios y 19.929
pacientes evaluó la temporización más adecuada
para la administración de inhibidores
de la glucoproteína IIb-IIIa (De Luca, Navarese,
& Cassetti, 2011).
Una estrategia de infusión temprano antes
de la admisión del paciente al laboratorio
de cateterización no fue capaz de reducir la
incidencia de la mortalidad a los 30 días o
AMI recurrente. Sin embargo, se asocia con
una mayor tasa de hemorragias graves.
Así, los inhibidores IIb-IIIa desempeñan un
papel importante como terapia adyuvante
en PCI, pero la prescripción de estos agentes
se limita a las situaciones no programados,
especialmente en el laboratorio de cateterismo,
con énfasis en los pacientes con
alto riesgo no del segmento ST elevación
ACS y sin tratamiento previo con P2Y12 inhibidores
del receptor, de la presencia de
complicaciones trombóticas durante la ICP
(abrupta oclusión de los vasos, lento flujo
epicárdico, la disección coronaria, rama
lateral oclusión) a IAM con elevación del
segmento ST en pacientes de alto riesgo
o en presencia de un aumento del trombótica
carga. Tras la consideración de estos
agentes, el perfil de riesgode los pacientes se debe considerar en relación con la ocurrencia
de eventos hemorrágicos, que son
conocidos promotores de aumento de la
morbilidad y la mortalidad.
Aunque el uso de inhibidores de la glicoproteína
IIb-IIIa tiene sin la influencia sobre
la eficacia de la nueva antiplaquetario oral
fármacos (ticagrelor, prasugrel) en el tratamiento
de ACS, se requiere más investigación
en cuanto a su uso en pacientes
tratados con el nuevo P2Y12 inhibidores
de los receptores, o aquellos con variantes
CYP2C19 genéticos o respuesta de baja
clopidogrel, o con respecto a la opción de
reducir o suprimir su dosis de mantenimiento.
d) El pretratamiento con P2Y12 antagonistas de los receptores
En la fase aguda de ACS, un escenario caracterizado
por un estado protrombótico
y la activación de plaquetas intenso, dual
aglutinación antiplaquetario representa un
importante paso terapéutico, y es intuitivo
para asumir que una acción potente y principios
farmacológica es capaz de conferir
eficacia anti-isquémica, reduciendo trombótica
eventos (infarto periprocedimiento,
trombosis del stent, reoclusión coronaria),
especialmente entre los pacientes sometidos
a la estratificación del riesgo invasivo
y PCI. Sin embargo, contrapuntos a un tratamiento
previo con P2Y12 antagonistas de
los receptores incluyen el aumento de la
prevalencia de complicaciones hemorrágicas
con la terapia antitrombótica, así como
un posible retraso en la aplicación de tratamiento
quirúrgico en pacientes con enfermedad
de múltiples vasos y la indicación
de la revascularización, la prolongación de
la duración de hospitalización y aumentar el
riesgo de hemorragia relacionado con la cirugía.
Aún así, hay escasas pruebas de los
ensayos clínicos aleatorios con la casuística
adecuada y el poder estadístico para obtener
una respuesta clara y definitiva a este
tema.
El juicio de clopidogrel para la reducción de es uno de los pioneros estudios que
sugieren un beneficio de principios antiplaquetaria
dual terapia inició inmediatamente
después del diagnóstico. Este ensayo
asignó al azar a 2.116 pacientes, incluyendo
66% diagnosticados con SCA (Wiviott,
Braunwald, & McCabe, 2007). El objetivo
del ensayo fue evaluar el beneficio de una
dosis de carga de 300 mg de clopidogrel
3-24 horas antes de la ICP y mantenimiento
de la doble terapia durante 12 meses. El
pretratamiento con clopidogrel se asoció
con una reducción no significativa del 18%
en el riesgo de muerte, IAM o revascularización
urgente en 28 días. Sin embargo, en un
análisis de subgrupos preespecificado, una
reducción significativa del 38,6% en el resultado
primario se observó en los pacientes
cuya terapia se inició 6 horas antes de
la ICP, la base conceptual para la adopción
de esta estrategia.
En la era de la nueva y potente P2Y12 inhibidores
de los receptores, el estudio Comparación
de Prasugrel en el momento de
coronaria percutánea intervención o como
pretratamiento en el momento del diagnóstico
en pacientes con no elevación del ST
infarto de miocardio (ACCOAST) asignó al
azar 4.033 pacientes con SCA sin elevación
del segmento ST para recibir una 30
mg dosis de prasugrel en el momento del
diagnóstico (pretratamiento), además de 30
mg en el caso de PCI, en comparación con
60 mg inmediatamente antes del procedimiento
(Montalescot, Bolognese, & Dudek,
2013). El primario punto final de eficacia,
compuesto de muerte cardiovascular, IAM,
ictus, revascularización urgente, o el uso no
planificado de inhibidores de la glucoproteína
IIb-IIIa a los 7 días no fue diferente entre
los grupos, mientras que el resultado de
seguridad, severa ocurrencia de sangrado
por la clasificación TIMI, era casi duplicará
entre aquellos tratados previamente con
prasugrel, con su uso en tales circunstancias
se desanimó.
e) La duración óptima de la terapia antiplaquetaria dual
Se recomienda la inhibición plaquetaria
doble durante un periodo de 1 año para
los pacientes diagnosticados de SCA, especialmente
aquellos que se sometieron
a cirugía de revascularización miocárdica
percutánea, con independencia del tipo de
stent; esta recomendación se basa en los
resultados de ensayos clínicos aleatorios
tales como CURE y, más recientemente,
TRITON-TIMI 38 y Platón, indicando una
beneficio temprana y continua de la terapia
antiplaquetaria dual de más de 12 meses
de tratamiento (Montalescot, van’t Hof, &
Lapostolle, Prehospital ticagrelor in ST-segment
elevation myocardial infarction., 2014).
Un tema reciente de la discusión es el mantenimiento
de la terapia antiplaquetaria dual
para más de 12 meses entre los individuos
sometidos a ICP. Un meta-análisis que abarca
seis ensayos clínicos aleatorios y 33,435
pacientes con una historia previa de IAM
mostró que la extensión de la doble antiagregación
después de 1 año promueve una
reducción significativa de eventos cardiovasculares
combinados comparación con
la monoterapia con AAS, lo que demuestra
una reducción aislada de muerte cardiovascular,
IAM, accidente cerebrovascular
y trombosis del stent a expensas de una
mayor incidencia de hemorragias graves
(Steinhubl, Tan, Foody, & Topol, 2009).
Conclusión
La farmacoterapia antiplaquetaria juega un
papel decisivo en la gestión clínica y invasivo
de ACS. El mayor conocimiento de la
fisiopatología de las cascadas que participan
en este proceso ha permitido la llegada
de los tipos más eficaces de tratamiento,
a menudo asociados con un mayor riesgo
de sangrado. Sin embargo, la seguridad
de cualquier prescripción es de suma importancia
en la práctica contemporánea, ya
que las complicaciones hemorrágicas conllevan
un alto riesgo de morbilidad y mortalidad.
Muchos estudios de investigación en curso siguen esta corriente tema controvertido,
y están sujetas a cambios regulatorios
constantes enfoques. Por lo tanto, siempre
por nosotros mismos guiar por el sentido
común, individualizado, y la estimación de
los riesgos y beneficios, que puede directamente
interferir en el pronóstico y la evolución
de los pacientes.
Bibliografía
Bolívar, J. (2015). Investigación Documental. México: Pax.
Bonello, L., Laine, M., Kipson, N., & Mancini, J.
(2014). Ticagrelor increases adenosine plasma
concentration in patients with acute coronary syndrome.
J Am Coll Cardiol, 872-7.
Castro, J. (2016). Técnicas Documentales. México: Limusa.
Chen, Z., Jiang, L., Chen, Y., Peto, R., Collins, R., &
Jiang, L. (2015). Addition of clopidogrel to aspirin
in 45,852 patients with acute myocardial infarction:
randomised placebo-controlled trial. Lancet,
1607-21.
Davila, A. (2015). Concepto de terminos cientificos. Caracas: Oasis.
De Luca, G., Navarese, E., & Cassetti, E. (2011). Metaanalysis of randomized trials of glycoprotein IIb/
IIIa inhibitors in high-risk acute coronary syndromes
patients undergoing invasive strategy. . Am J
Cardiol., 198-203.
Fuster, V., & Sweeny, J. (2011). Aspirin: a historical
and contemporary therapeutic overview. . Circulation.,
768-78.
Holmes, D. J., & Dehmer, G. (2010). ACCF/AHA
clopidogrel clinical alert: approaches to the FDA
“boxed warning: ” a report of the American College
of Cardiology Foundation Task Force on Clinical
Expert Consensus Documents and and the
American Heart Association. . J Am Coll Cardiol.,
56.
ISIS-2 (Second International Study of Infarct Survival).
(1988). Collaborative Group. Randomised
trial of intravenous streptokinase, oral aspirin,
both, or neither among 17 187 cases of suspected
acute myocardial infarction. Lancet, 349-60.
Montalescot, G., Bolognese, L., & Dudek, D. (2013).
ACCOAST Investigators. Pretreatment with prasugrel
in non-ST-segment elevation acute coronary
syndromes. N Engl J Med., 999-1010.
Montalescot, G., van’t Hof, A., & Lapostolle, F. (2014).
Prehospital ticagrelor in ST-segment elevation
myocardial infarction. N Engl J Med. , 1016–27.
Moussa, S., & Bennet, J. (2006). Platelets in health
and disease: platelet GP IIb/IIIa structure and
function: recent advances in antiplatelet therapy. .
Drugs Future, 1141-54.
Patrono, C., Baigent, C., Hirsh, J., & Roth, G. (2008).
Antiplatelet drugs: American College of Chest Physicians
Evidence-Based Clinical Practice Guidelines.
Chest , 199S-233S.
Piegas, L., Avezum, A., & Guimarães, H. (2013).
Acute coronary syndrome behavior: results of a
Brazilian registry. Arq Bras Cardiol, 502-10.
Sabatine, M., Cannon, C., Gibson, C., López-Sendón,
J., Montalescot, G., & Theroux, P. (2005).
CLARITY-TIMI 28 Investigators. Addition of clopidogrel
to aspirin and fibrinolytic therapy for myocardial
infarction with ST-segment elevation. N
Engl J Med., 352.
Steinhubl, S., Tan, W., Foody, J., & Topol, E. (2009).
Incidence and clinical course of thrombotic thrombocytopenic
purpura due to ticlopidine following
coronary stenting. EPISTENT Investigators. Evaluation
of Platelet IIb/ IIIa Inhibitor for Stenting.
JAMA, 3-25.
Vedanthan, R., Seligman, B., & Fuster, V. (2014). Global
perspective on acute coronary syndrome: a
burden on the young and poor. Circ Res, 1959-75.
Wallentin, L., Becker, R., & Budaj, A. (2009). Ticagrelor
versus clopidogrel in patients with acute coronary
syndromes. N Engl J Med, 1045-57.
Wiviott, S., Braunwald, E., & McCabe, C. (2007). Prasugrel
versus clopidogrel in patients with acute coronary
syndrome. N Engl J Med, 2001-15.
Yusuf, S., Zhao, F., Metha, S., Chrolavicius, S., Toçnoni,
G., & Fox, K. (2001). The clopidogrel in unstable
angina to prevent recurrent events trial investigators.
Effects of clopidogrel in addition to aspirin in
patients with acute coronary syndromes without
ST-segment elevation. N Engl J Med, 494-502.

Reconocimiento-NoComercial-CompartirIgual
CC BY-NC-SA
Esta licencia permite a otros entremezclar, ajustar y construir a partir de su obra con fines no comerciales, siempre y cuando le reconozca la autoría y sus nuevas creaciones estén bajo una licencia con los mismos términos.




